純物質的飽和蒸氣壓與溫度間的函數關係式。在一定溫度下,液態和固態的純物質都有相應的飽和蒸氣壓。當溫度升高時,飽和蒸氣壓大體呈指數關係上升。採用僅含少量參數的蒸氣壓方程關聯飽和蒸氣壓與溫度資料,可以概括大量實驗資訊。這樣便於資料的收集、貯存和取用。飽和蒸氣壓是重要的化工基礎資料,常用於標準態逸度、蒸發熱、昇華熱(見熱化學資料)及相平衡關聯等方面的計算。
早期的蒸氣壓方程有1794年提出的普羅尼方程:
 1841年提出的雷德方程:
1841年提出的雷德方程:
 兩者都是經驗方程。以上兩式中
p°為飽和蒸氣壓;
t為攝氏溫度;
A、
B、
C、
α、
β和γ 均為方程參數。1834年,法國化學傢B.-P.-É.克拉珀龍分析瞭包含
汽液平衡的卡諾循環後,提出飽和蒸氣壓的理論方程。1850年德國化學傢R.克勞修斯為此方程作瞭嚴格的熱力學推導,並把它推廣到其他
相平衡系統。此方程後來稱為克勞修斯-克拉珀龍方程,其表達式為:
兩者都是經驗方程。以上兩式中
p°為飽和蒸氣壓;
t為攝氏溫度;
A、
B、
C、
α、
β和γ 均為方程參數。1834年,法國化學傢B.-P.-É.克拉珀龍分析瞭包含
汽液平衡的卡諾循環後,提出飽和蒸氣壓的理論方程。1850年德國化學傢R.克勞修斯為此方程作瞭嚴格的熱力學推導,並把它推廣到其他
相平衡系統。此方程後來稱為克勞修斯-克拉珀龍方程,其表達式為:
 式中
p為相平衡時的壓力,Δ
H為相變熱,Δ
V為相變時的體積變化,
T為絕對溫度。
式中
p為相平衡時的壓力,Δ
H為相變熱,Δ
V為相變時的體積變化,
T為絕對溫度。
在用於汽液或汽固相變化時,對ΔH/ΔV作不同的簡化,可以得到不同的蒸氣壓方程,常用的有:
①克拉珀龍方程 由克拉珀龍提出:
lnp°=A-B/T
式中 A和 B為特征參數。這是最簡單的蒸氣壓方程,適用於溫度遠低於臨界溫度的場合;但在用於正常沸點(101.325kPa下的沸點)以下時,計算值通常偏高,且一般不適用於締合液體(如醇類)。將此方程用臨界溫度 Tc(此時飽和蒸氣壓為臨界壓力 pc) 和正常沸點 T b(此時飽和蒸氣壓為101.325kPa)消去 A和 B,可得到普遍化蒸氣壓方程: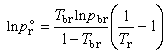 式中
p
r
o=
p°/
pc;
T
r=
T/
Tc;
p
式中
p
r
o=
p°/
pc;
T
r=
T/
Tc;
p
 =101.325/
pc;
T
=101.325/
pc;
T
 =
T
b/
Tc(見
對應態原理)。為瞭提高計算準確度,可引入第三參數偏心因子
ω,得:
=
T
b/
Tc(見
對應態原理)。為瞭提高計算準確度,可引入第三參數偏心因子
ω,得:
lnpro=f[0](Tr)+ωf[1](Tr)
式中 f [0]和 f [1]為 T r的普適函數。在 T b到 Tc范圍內,該式誤差通常在1%~2%之內;在溫度低於 T b時,計算值可能偏低百分之幾。②安托因方程 由C.安托因提出:
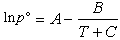 式中
A、
B和
C均為特征參數,又稱安托因常數。許多物質的安托因常數列於物性手冊中,適用的溫度范圍相當於飽和蒸氣壓范圍為1.5~200kPa,一般不宜外推。
式中
A、
B和
C均為特征參數,又稱安托因常數。許多物質的安托因常數列於物性手冊中,適用的溫度范圍相當於飽和蒸氣壓范圍為1.5~200kPa,一般不宜外推。
蒸氣壓方程中,蒸氣壓僅是溫度的單變量函數,因而隻適用於不存在表面張力、流體靜壓力、重力和電磁場等的影響時。一般在化工計算中,上述影響可不考慮。但當液體表面曲率不容忽略時(如蒸氣冷凝形成液滴時),就要考慮表面張力的影響。當流體靜壓力較大時(如液面有高壓惰性氣體作用時),也要考慮壓力的影響。