生成酯的反應過程。酯是一類重要的有機化工產品,除本身是溶劑、增塑劑而用於很多工業部門外,還大量用來生產聚酯,也有一部分用作有機合成的原料。酯類生產的歷史悠久,其基礎理論的研究也早已開始,英國化學傢A.W.威廉森在1852年已經提出瞭由酸與醇合成酯的理論。
可生成酯的方法很多,工業上應用最廣的是直接酯化和酯基轉移。此外,還有一些適用於生產某些特定酯的過程。
直接酯化 羧酸與醇反應生成酯和水:
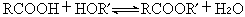 這是一個可逆反應,通常熱效應較小。正向反應稱為直接酯化反應,逆向反應則為
水解。酯化反應的平衡常數主要取決於酸和醇的性質,而與溫度的關系不大。例如:酸與同一碳數的醇進行酯化反應時,以伯醇的平衡常數最大,仲醇次之,叔醇最小。直接酯化反應速度很慢,隻有在催化劑的存在下,才能獲得有工業意義的反應速度。常用的催化劑有硫酸、鹽酸、陽離子交換樹脂等。工業上很多重要的酯是由直接酯化獲得的,如對苯二甲酸酯等。事實上,隻要由相應的酸和醇可以直接獲得酯,直接酯化總是首先被考慮采用的方法。
這是一個可逆反應,通常熱效應較小。正向反應稱為直接酯化反應,逆向反應則為
水解。酯化反應的平衡常數主要取決於酸和醇的性質,而與溫度的關系不大。例如:酸與同一碳數的醇進行酯化反應時,以伯醇的平衡常數最大,仲醇次之,叔醇最小。直接酯化反應速度很慢,隻有在催化劑的存在下,才能獲得有工業意義的反應速度。常用的催化劑有硫酸、鹽酸、陽離子交換樹脂等。工業上很多重要的酯是由直接酯化獲得的,如對苯二甲酸酯等。事實上,隻要由相應的酸和醇可以直接獲得酯,直接酯化總是首先被考慮采用的方法。
反應機理 直接酯化是由羧酸提供羥基,經過四面體中間物的反應過程。以酯酸和乙醇反應為例:
 首先是把羧酸的羧基質子化,使(1)帶有更多的正電性,容易與醇發生親核加成,形成一個四面體中間物(2),然後質子轉移為(3),進而脫水成(4),最後消除質子而形成酯(5)。因此,直接酯化反應的速度與酸、醇以及催化劑(或
H
+)的濃度成正比,同時與反應物的分子結構有關。高級異構醇(及酸)因位阻效應,其直接酯化反應速度過小,不宜采用直接酯化方法生產相應的酯。
首先是把羧酸的羧基質子化,使(1)帶有更多的正電性,容易與醇發生親核加成,形成一個四面體中間物(2),然後質子轉移為(3),進而脫水成(4),最後消除質子而形成酯(5)。因此,直接酯化反應的速度與酸、醇以及催化劑(或
H
+)的濃度成正比,同時與反應物的分子結構有關。高級異構醇(及酸)因位阻效應,其直接酯化反應速度過小,不宜采用直接酯化方法生產相應的酯。
工藝方法 工業上絕大多數直接酯化過程均為液相反應,由於受平衡限制,反應不能進行完全,故常用從反應混合物中移走反應產物(水,酯或兩者在一起)的辦法來移動平衡點。常用的有三種方法:①直接從反應物中蒸出酯,適用於生成的酯的揮發度比原料醇大的場合。例如:生產甲酸甲酯、乙酸甲酯、甲酸乙酯等。②蒸出酯-水共沸物,適用於生成中等揮發度的酯,例如生產甲酸丙酯、甲酸丁酯、醋酸乙酯、醋酸丙酯等,它們與水形成共沸物被蒸出。③當生成的酯揮發度較低時,須外加共沸劑(通常為苯、甲苯等)或利用醇本身,使之與水形成共沸物而將水移出反應混合物。反應器可以是連續式的或間歇式的。間歇式反應器通常為帶攪拌的反應釜;連續式反應器則是塔式的。為防止無機酸催化劑對設備的腐蝕,須妥善選擇反應器的材質及結構。
酯基轉移 使酯與羧酸、醇或另一種酯反應獲得所需的酯的反應過程:
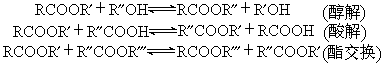
酯基轉移反應一般為可逆反應,其熱效應較相應的直接酯化更小。平衡常數主要取決於羧酸、醇、酯的分子結構,其一般規律與直接酯化相似。工業上多在催化劑存在下在液相中進行。用於直接酯化的催化劑也可用於酯基轉移。但對於醇解及酯交換,采用堿催化劑(如醇鈉)較酸催化劑更能加快反應速度,這是因為兩者的反應機理不同。用酸催化劑時,反應機理與直接酯化時類似。而在堿催化劑存在下,由於醇中的氧原子堿性增大,能直接攻擊羧基上的碳原子,酯中的酰基或烷氧基上的吸電子取代基團的反應速度均將增加。而反應活化能較小。工業上為使反應的平衡點轉移,可移走反應產物之一(一般用蒸發或沉淀的方法均可),也常用加適量酸或醇的辦法。
酯基轉移在工業應用上的重要實例是:由甲基丙烯酸甲酯或其他酯與高級醇進行醇解而制得甲基丙烯酸的高級醇酯;聚醋酸乙烯酯與甲醇反應得聚乙烯醇;對苯二甲酸甲酯與乙二醇反應得對苯二甲酸乙二酯;以及由甘油與相應的脂肪酸反應得不飽和脂肪酸的單甘油酯等。
應用較少的酯化過程 主要有:
① 酸酐與醇的反應:
 因為沒有水生成,不會發生逆反應。一般是用三氟乙酸、氯化鋅、氯化鐵等為催化劑,反應在液相中進行。由於酐的價格較貴,故隻在不能由酸直接酯化時才采用。工業上大規模應用的實例是由醋酸酐生產
醋酸纖維素。
因為沒有水生成,不會發生逆反應。一般是用三氟乙酸、氯化鋅、氯化鐵等為催化劑,反應在液相中進行。由於酐的價格較貴,故隻在不能由酸直接酯化時才采用。工業上大規模應用的實例是由醋酸酐生產
醋酸纖維素。
② 羧酸與乙炔加成:
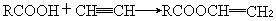 是專門用來生產乙烯酯的方法。對低級羧酸,可在鋅或汞鹽存在下進行氣相反應;對高級羧酸則常采用液相法,以氧化汞/硫酸為催化劑(例如由乙炔與硬脂酸生產硬脂酸乙烯酯)。
是專門用來生產乙烯酯的方法。對低級羧酸,可在鋅或汞鹽存在下進行氣相反應;對高級羧酸則常采用液相法,以氧化汞/硫酸為催化劑(例如由乙炔與硬脂酸生產硬脂酸乙烯酯)。
③ 酰氯、酰胺或腈與醇的反應:
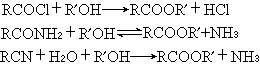 這些方法均隻在個別情況下使用。
這些方法均隻在個別情況下使用。
參考書目
P.H.Groggins,Unit Processes in Organic Synth-esis,5th ed.,McGraw-Hill,New York.1958.