CH3CHO 無色、易揮發並具有刺激性氣味的液體,沸點20.8°C,可溶於水。其蒸氣易燃,可與空氣形成爆炸混合物(4%~60%體積)。在空氣中易氧化,貯存和運輸中需充氮。主要由乙烯氧化制得,是合成多種有機化工產品的原料。
1774年,瑞典化學傢K.W.舍勒以乙醇、二氧化錳和硫酸反應首先制得乙醛。1881年,俄國人Μ.Γ.庫切羅夫將乙炔通入高價汞鹽的的硫酸溶液也制得瞭乙醛。庫切羅夫的工作為1916年乙炔水合制乙醛的工業化奠定瞭基礎。此後,長時期內乙炔水合法曾是生產乙醛的唯一工業化方法,但所用催化劑有毒。1940和1959年又先後開發成功瞭乙醇氧化法和乙烯直接氧化法,大大促進瞭乙醛的生產。
生產方法 工業上主要有乙烯直接氧化法、乙醇氧化法和乙炔水合法。此外,還有丙烷或丙烷、丁烷混合物氧化制乙醛及其他含氧化合物的方法,由於產物組成復雜,分離困難,未能得到推廣。
乙烯直接氧化法 又稱瓦克法,它是世界上第一個采用均相配位催化劑實現工業化的過程,此法的成功一方面促進瞭乙醛的生產,另一方面對均相配位催化理論的發展具有重要意義。該法以氯化鈀-氯化銅-鹽酸-水組成的溶液為催化劑(見絡合催化劑),使乙烯直接氧化為乙醛。總反應式為:
 實際反應按下述兩步進行:
實際反應按下述兩步進行:
① 乙烯的氧化:
CH2=CH2+PdCl2+H2O─→CH3CHO+Pd+2HCL
② 催化劑溶液的氧化再生:
Pd+2CuCl2─→PdCl2+2CuCl
 工業上有將上述兩步反應過程安排在一個反應器中進行的一步法(圖1)和分別安排在兩個反應器中完成的兩步法(圖2)兩種生產流程。
工業上有將上述兩步反應過程安排在一個反應器中進行的一步法(圖1)和分別安排在兩個反應器中完成的兩步法(圖2)兩種生產流程。
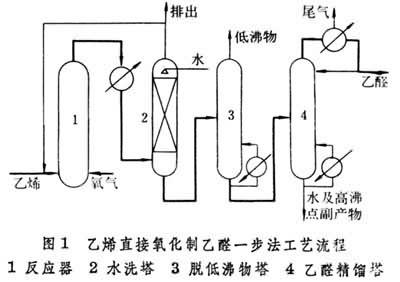
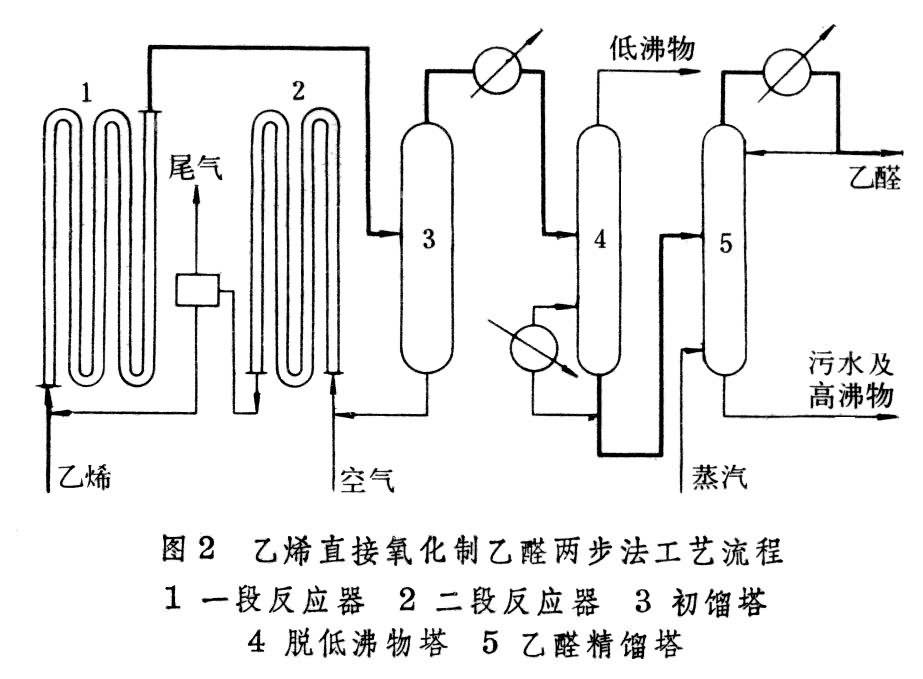
一步法以氧氣為氧化劑,氧氣和乙烯同時通入裝有催化劑溶液的塔式反應器。依靠催化劑溶液中水的蒸發和產物的移出帶走反應熱,維持120~130°C、0.4~0.45MPa的反應條件使乙烯氧化為乙醛。兩步法以空氣為氧化劑,乙烯和催化劑溶液一起通入一段反應器,在100~110°C、1.0~1.2MPa下乙烯進行氧化反應生成乙醛;分去產物後的催化劑溶液經補充損失的水後進入到二段反應器,用空氣進行氧化再生。兩種方法的乙醛收率均為95%左右,但一步法流程簡單、投資少,是目前世界上絕大多數國傢采用的方法。兩步法的優點是不需空氣分離裝置、乙烯轉化率高、對乙烯純度要求低和反應後氣體不需循環等,但催化劑循環要消耗能量。
乙醇氧化法 以空氣為氧化劑。乙醇蒸氣和空氣經混合和加熱至460°C左右自頂部進入裝有銀催化劑的固定床反應器,進行氧化脫氫反應生成乙醛:

此過程的主要副反應是乙醛繼續氧化為醋酸:
 為移走反應熱,催化劑床層中設有用水冷卻的盤管。反應產物經冷卻、冷凝和水洗即得粗乙醛溶液,粗乙醛通過精餾分離可得各種純度的乙醛產品。此法操作簡單、乙醛收率高。但生產能力受乙醇來源和價格的限制。
為移走反應熱,催化劑床層中設有用水冷卻的盤管。反應產物經冷卻、冷凝和水洗即得粗乙醛溶液,粗乙醛通過精餾分離可得各種純度的乙醛產品。此法操作簡單、乙醛收率高。但生產能力受乙醇來源和價格的限制。
乙炔水合法 以乙炔為原料,在汞鹽催化劑存在下,於70~90°C的硫酸溶液中水合而得乙醛:
CH≡CH+H2O─→CH3CHO
其工藝過程主要包括乙炔水合制粗乙醛、粗乙醛精餾和催化劑回收三部分。此法的特點是反應條件緩和、乙醛收率高,但所用催化劑有毒,反應介質對設備有較強的腐蝕性,環境污染嚴重。已逐漸被其他方法所取代。用途 最大用途是制造醋酸和醋酐,約占總量的50%~70%。近年隨甲醇羰化(見羰基合成)合成醋酸過程的開發,乙醛作為合成醋酸原料的需要量下降,並影響乙醛產量。乙醛也較多地用於制造醋酸乙酯、正丁醇、2-乙基己醇,後兩個產品也有被丙烯的羰基合成法所取代的趨勢。乙醛還用於生產三氯乙醛、吡啶、季戊四醇等。